2.5: Cyclohexane : Un cycloalcane sans tension
- Page ID
- 126840
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)
Les anneaux plus grands que le cyclopentane auraient une tension angulaire s'ils étaient plans. Cependant, cette contrainte, ainsi que la contrainte d'éclipse inhérente à une structure plane, peuvent être soulagées en pliant l'anneau. Le cyclohexane est un bon exemple de système carbocyclique qui élimine virtuellement l'éclipse et la tension angulaire en adoptant des conformations non-planaires. Le cycloheptane et le cyclooctane sont plus sollicités que le cyclohexane, en grande partie à cause de l'encombrement transannulaire (entrave stérique par des groupes situés sur les côtés opposés de l'anneau).
Conformations du cyclohexane
Une structure plane pour le cyclohexane est clairement improbable. Les angles de liaison seraient nécessairement de 120º, soit 10,5º de plus que l'angle tétraédrique idéal. De plus, toute liaison carbone-carbone dans une telle structure serait éclipsée. L'angle qui en résulterait et les tensions qui s'éclipseraient déstabiliseraient gravement cette structure. Si deux atomes de carbone sur les côtés opposés de l'anneau à six membres sont soulevés hors du plan de l'anneau, une grande partie de la contrainte angulaire peut être éliminée.
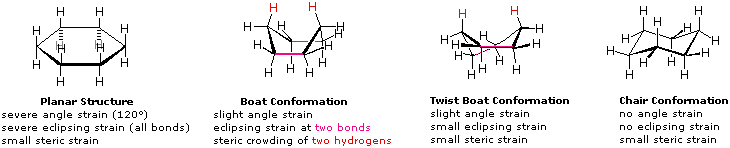
Cette structure de bateau a encore deux liaisons éclipsées et un encombrement stérique important de deux atomes d'hydrogène sur la "proue" et la "poupe" du bateau. Cet encombrement stérique est souvent appelé obstacle stérique. En tordant la conformation du bateau, l'obstacle stérique peut être partiellement levé, mais le conformiste conserve encore certaines des contraintes qui caractérisent le conformiste du bateau. Enfin, en soulevant un carbone au-dessus du plan de l'anneau et l'autre au-dessous du plan, un conformateur de " chaise " relativement sans contrainte est formé. C'est la structure prédominante adoptée par les molécules de cyclohexane.
Confirmations "Bateau" vs. "Chaise"
Après un examen attentif de la conformation d'une chaise en cyclohexane, nous constatons que les douze hydrogènes ne sont pas structurellement équivalents. Six d'entre eux sont situés à la périphérie de l'anneau de carbone, et sont appelés équatoriaux. Les six autres sont orientés au-dessus et au-dessous du plan approximatif de l'anneau (trois à chaque endroit), et sont appelés axiaux parce qu'ils sont alignés parallèlement à l'axe de symétrie de l'anneau.
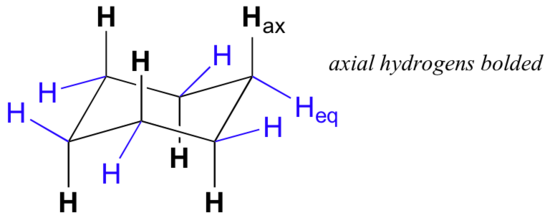
Dans la figure ci-dessus, les hydrogènes équatoriaux sont colorés en bleu et les hydrogènes axiaux sont en gras. Puisqu'il existe deux conformations de chaise équivalentes de cyclohexane en équilibre rapide, les douze hydrogènes ont un caractère équatorial de 50 % et axial de 50 %. La figure ci-dessous illustre comment convertir un modèle moléculaire de cyclohexane entre deux conformations de chaise différentes - c'est quelque chose que vous devriez pratiquer avec des modèles. Remarquez qu'un "ring flip" fait que les hydrogènes équatoriaux deviennent axiaux, et vice-versa.
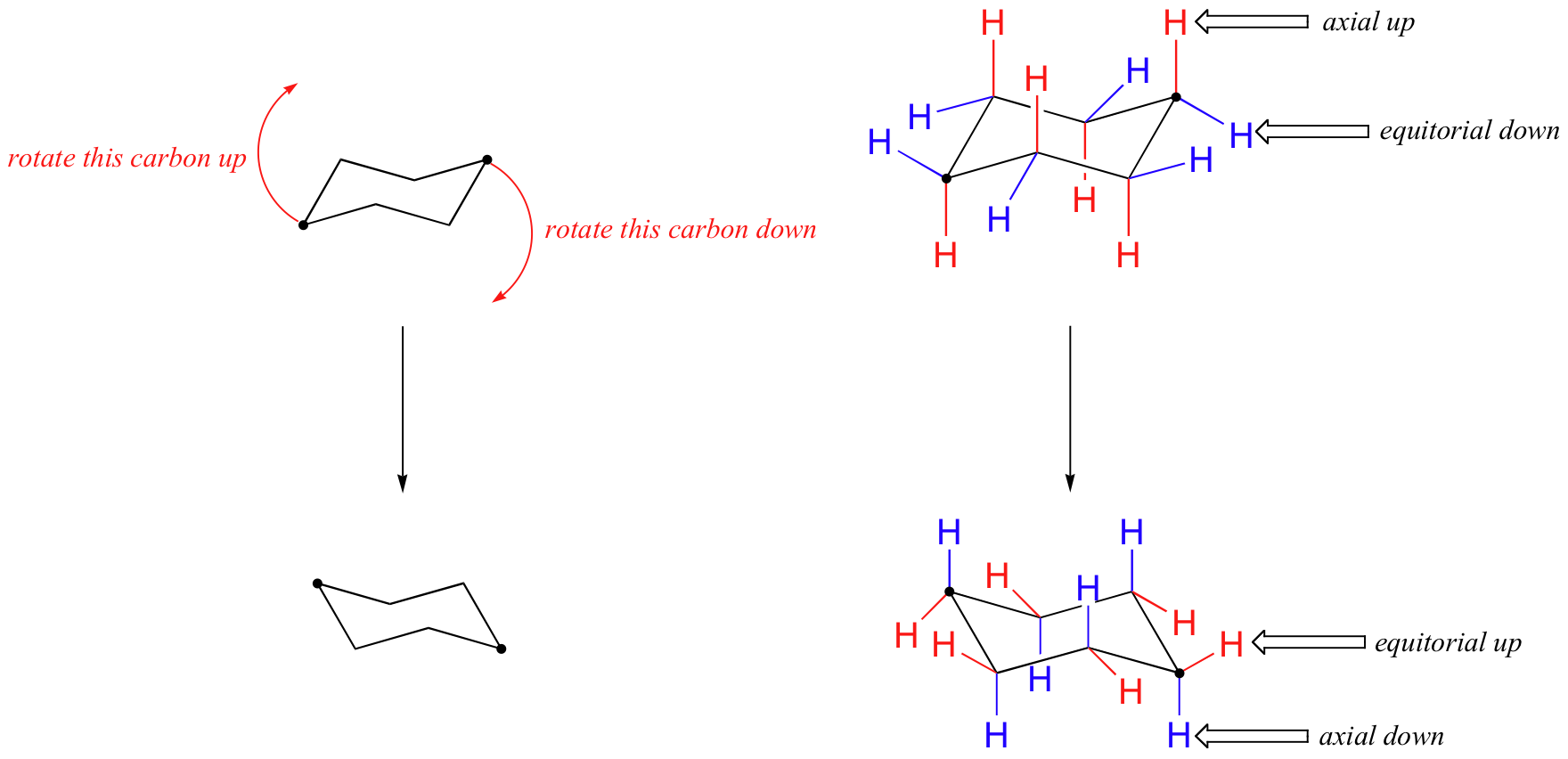
Comment dessiner des chaises
En plus de dessiner la chaise de base, les points clés pour ajouter des substituants sont :
- Les groupes axiales alternent vers le haut et vers le bas et sont représentés "verticalement".
- Les groupes équatoriaux sont approximativement horizontaux, mais en fait quelque peu déformés, de sorte que l'angle du groupe axial est un peu plus qu'un angle droit - reflétant l'angle de liaison commun de 109 degrés.
- Comme nous l'avons déjà dit, il est généralement plus facile de dessiner et de voir ce qui se passe aux quatre coins de la chaise qu'aux deux positions centrales. Essayez d'utiliser les coins autant que possible.
Parce que les liaisons axiales sont parallèles les unes aux autres, les substituants plus grands que l'hydrogène souffrent généralement d'un encombrement stérique plus important lorsqu'ils sont orientés axialement plutôt qu'équatorial. Par conséquent, les cyclohexanes substitués adopteront de préférence des conformations dans lesquelles les plus grands substituants prennent une orientation équatoriale.
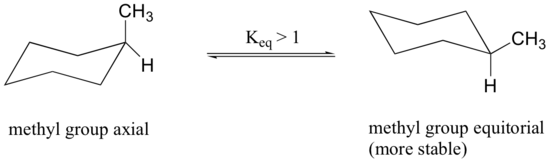
Lorsque le groupe méthyle dans la structure ci-dessus occupe une position axiale, il subit un encombrement stérique par les deux hydrogènes axiaux situés du même côté de l'anneau.

La conformation dans laquelle le groupe méthyle est équatorial est plus stable, et donc l'équilibre se situe dans cette direction

