3.1: Molécules chirales
- Page ID
- 126848
Les stéréoisomères sont des isomères dont la configuration spatiale des atomes diffère, plutôt que l'ordre de connectivité atomique. L'un de leurs types d'isomères les plus intéressants est le stéréo-isomères à image miroir, un ensemble non superposable de deux molécules qui sont des images miroir l'une de l'autre. L'existence de ces molécules est déterminée par un concept connu sous le nom de chiralité. Le mot "chiral" est dérivé du mot grec "main", parce que nos mains montrent un bon exemple de chiralité puisqu'il s'agit d'images miroir non superposables les unes aux autres.
Introduction
Le contraire de chiral est achiral. Les objets achiraux sont superposables avec leurs images miroirs. Par exemple, deux feuilles de papier sont achiral. En revanche, les molécules chirales, comme nos mains, sont des images miroir non superposables les unes des autres. Essayez d'aligner parfaitement votre main gauche avec votre main droite, de sorte que les paumes des mains soient tournées dans la même direction. Passez une minute à faire ça. Voyez-vous qu'ils ne peuvent pas s'aligner exactement ? La même chose s'applique à certaines molécules.
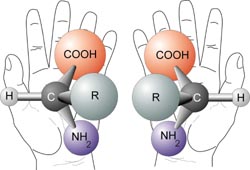
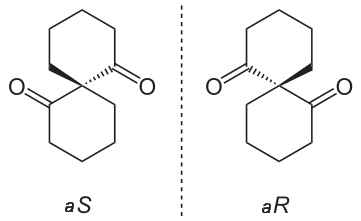
Une molécule chirale a une image miroir qui ne peut pas s'aligner parfaitement avec elle - les images miroir ne sont pas superposables. Les images miroirs sont appelées énantiomères. Mais pourquoi les molécules chirales sont-elles si intéressantes ? Une molécule chirale et son énantiomère ont les mêmes propriétés chimiques et physiques (point d'ébullition, point de fusion, polarité, densité etc...). Il s'avère que bon nombre de nos molécules biologiques, comme notre ADN, nos acides aminés et nos sucres, sont des molécules chirales.
Il est assez intéressant de constater que nos mains semblent servir le même but, mais la plupart des gens ne sont capables d'utiliser qu'une seule de leurs mains pour écrire. C'est également le cas des molécules biologiques chirales et de leurs interactions. Tout comme votre main gauche ne rentre pas correctement dans votre gant droit, l'un des énantiomères d'une molécule peut ne pas fonctionner de la même façon dans votre corps.
Cela doit signifier que les énantiomères ont des propriétés qui les rendent uniques à leurs images miroirs. L'une de ces propriétés est qu'ils ne peuvent pas avoir un plan de symétrie ou un plan miroir interne. Ainsi, une molécule chirale ne peut pas être divisée en deux moitiés d'image miroir. Une autre propriété des molécules chirales est l'activité optique.
Les composés organiques, molécules créées autour d'une chaîne d'atomes de carbone (plus communément appelée squelette carbone), jouent un rôle essentiel dans la chimie de la vie. Ces molécules tirent leur importance de l'énergie qu'elles transportent, principalement sous forme d'énergie potentielle entre molécules atomiques. Étant donné que cette force potentielle peut être largement affectée par des changements dans le placement atomique, il est important de comprendre le concept d'un isomère, une molécule partageant la même composition atomique qu'une autre mais ayant des dispositions structurelles différentes. Cet article sera consacré à un isomère spécifique appelé stéréoisomère et à sa propriété de chiralité (Figure 5.1.1).
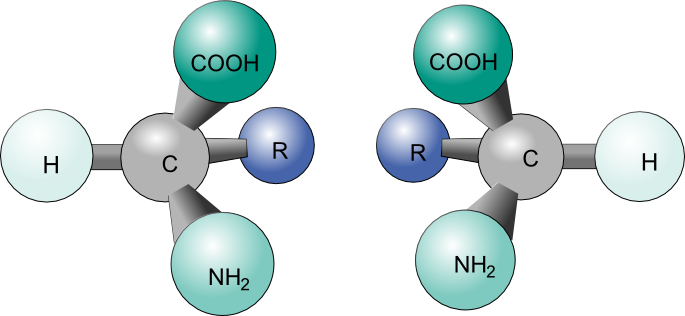
Figure 5.1.1. Deux énantiomères d'un complexe tétraédrique. Image utilisée avec la permission de Wikipedia
Les concepts de stéréoisomérisme et de chiralité revêtent une grande importance dans la chimie organique moderne, car ces idées aident à comprendre les raisons physiques et théoriques de la formation et de la structure de nombreuses molécules organiques, raison principale de l'énergie contenue dans ces produits chimiques essentiels. Contrairement à l'isomérisme constitutionnel plus connu, qui développe des composés isotopiques simplement par une connectivité atomique différente, le stéréoisomérisme maintient généralement des connexions atomiques et des ordres de blocs de construction égaux ainsi qu'un même nombre d'atomes et de types d'éléments.
Qu'est-ce qui rend les stéréoisomères si uniques ? Pour répondre à cette question, l'apprenant doit être capable de penser et d'imaginer non seulement en images bidimensionnelles, mais aussi en espace tridimensionnel. Ceci est dû au fait que les stéréoisomères sont des isomères parce que leurs atomes sont différents des autres en termes d'arrangement spatial.
Arrangement spatial
Il faut d'abord et avant tout comprendre le concept d'agencement spatial pour comprendre le stéréoisomérisme et la chiralité. L'arrangement spatial des atomes concerne la façon dont les différentes particules et molécules atomiques sont situées dans l'espace autour du composé organique, à savoir sa chaîne carbonée. En ce sens, la disposition spatiale d'une molécule organique est différente l'une de l'autre si un atome est déplacé dans une direction tridimensionnelle d'un seul degré. Cela ouvre une très large possibilité de molécules différentes, chacune avec son placement unique d'atomes dans l'espace tridimensionnel.
Stéréoisomères
Les stéréoisomères sont, comme mentionné ci-dessus, contiennent différents types d'isomères en eux-mêmes, chacun ayant des caractéristiques distinctes qui se séparent en entités chimiques différentes ayant des propriétés différentes. Les types appelés entaniomères sont les stéréoisomères à image miroir mentionnés précédemment, et seront expliqués en détail dans cet article. Un autre type, le diastéréoisomère, a des propriétés différentes et sera introduit par la suite.
Enantiomères
Ce type de stéréoisomère est le type essentiel de stéréoisomère à image miroir, non superposable, présenté au début de l'article. La figure 3 en est un parfait exemple ; notez que le plan gris au milieu rétrograde le plan miroir.
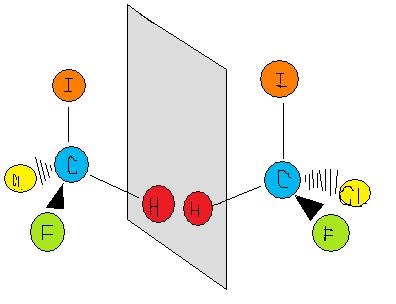
Figure 5.1.2.
Notez que même si l'on retournait la molécule de gauche vers la droite, l'arrangement spatial atomique ne serait pas égal. C'est l'équivalent de la relation main gauche - main droite, que l'on appelle à juste titre " main droite " dans les molécules. Cela peut être quelque peu contre-intuitif, c'est pourquoi cet article recommande au lecteur d'essayer l'exemple de la " main ". Placez la paume de la main vers le haut et les mains l'une à côté de l'autre. Maintenant, retournez l'un ou l'autre côté de l'autre côté. Une main devrait montrer le dos de la main, tandis que l'autre montre la paume. Ils ne sont pas les mêmes et ne sont pas superposables. C'est là que le concept de chiralité entre en jeu comme l'une des idées les plus essentielles et déterminantes du stéréoisomérisme.
Chiralité
Chiralité signifie essentiellement'molécules miroir-image, non-superposables', et dire qu'une molécule est chirale, c'est dire que son image miroir (elle doit en avoir une) n'est pas la même que la sienne. Qu'une molécule soit chirale ou achirale dépend d'un certain nombre de conditions qui se chevauchent. La figure 5.1.1.1 montre un exemple de deux molécules, chirale et achirale, respectivement. Remarquez la caractéristique distincte de la molécule achirale : elle possède deux atomes d'un même élément. En théorie et en réalité, si l'on devait créer un plan qui traverse les deux autres atomes, ils seraient capables de créer ce qu'on appelle un plan bissectrice : Les images de chaque côté du plan sont les mêmes que l'autre (Figure 5.1.3).
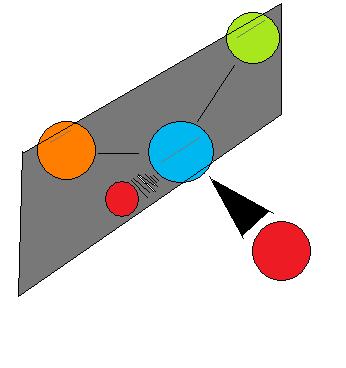
Figure 5.1.3.
Dans ce cas, la molécule est considérée comme " achirale ". En d'autres termes, pour distinguer une molécule chirale d'une molécule achirale, il faut rechercher l'existence du plan bissectrice dans une molécule. Toutes les molécules chirales sont dépourvues de plan bissectrice, qu'il soit simple ou complexe. En règle générale, aucune molécule ayant des atomes environnants différents n'est achirale. La chiralité est une idée simple mais essentielle pour soutenir le concept de stéréoisomérisme, étant utilisé pour expliquer un type de ce genre. Les propriétés chimiques de la molécule chirale diffèrent de son image miroir, d'où l'importance de la chilarité par rapport à la chimie organique moderne.

